2-Metilhekzan
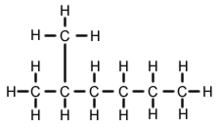
2-metilhekzan (C7,H16, aynı zamanda izoheptan, etilizobütilmetan olarak da bilinir) bir heptan izomeridir. Yapısal olarak ikinci karbon atomuna bağlı bir metil grubu olan bir hekzan molekülüdür. Ticari olarak temin edilebilen heptan ürünlerinde safsızlık olarak bulunur, ancak n-heptan (düz zincirli heptan) ile karşılaştırıldığında çok benzer fiziksel ve kimyasal özelliklere sahip olduğu için genellikle reaksiyonlar açısından safsızlık olarak kabul edilmez.

| |
| |

| |
| Adlandırmalar | |
|---|---|
| Tanımlayıcılar | |
3D model (JSmol)
|
|
| 1696856 | |
| ChemSpider | |
| ECHA InfoCard | 100.008.847 |
| EC Numarası |
|
PubChem CID
|
|
| RTECS numarası |
|
| UN numarası | 3295 |
CompTox Bilgi Panosu (EPA)
|
|
| |
| |
| Özellikler | |
| Kimyasal formül | C7H16 |
| Molekül kütlesi | 100,20 g mol−1 |
| Görünüm | Renksiz sıvı |
| Yoğunluk | 0.679 g cm−3 |
| Erime noktası | 154,1 °C'den 155,3 °C'ye |
| Kaynama noktası | 362,7 °C'den 363,7 °C'ye |
| Buhar basıncı | 15,7 kPa (37,7 °C'de) |
Henry yasası
sabiti (kH) |
19 nmol Pa−1 kg−1 |
| Termokimya | |
Isı sığası (C)
|
222,92 J K−1 mol−1 |
Standart molar entropi (S⦵298)
|
323,34 J K−1 mol−1 |
Standart formasyon entalpisi (ΔfH⦵298)
|
−231,1–−228,5 kJ mol−1 |
Standart yanma entalpisi (ΔcH⦵298)
|
−4,8127–−4,8103 MJ mol−1 |
| Tehlikeler | |
| GHS etiketleme sistemi: | |
| Piktogramlar |    
|
| İşaret sözcüğü | TEHLİKE |
| Tehlike ifadeleri | H225, H304, H315, H336, H410 |
| Önlem ifadeleri | P210, P261, P273, P301+P310, P331 |
| NFPA 704 (yangın karosu) |
|
| Parlama noktası | −1 |
| 280 | |
| Patlama sınırları | %1-7 |
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa).
| |
| Bilgi kutusu kaynakları | |
Bir alkan olarak, 2-metılhekzan, su içinde çözünmez, ancak alkoller ve etergibi birçok organik çözücü içinde çözünür. Bununla birlikte, 2-metilhekzan daha çok bir çözücü olarak kabul edilir. Bu nedenle, ticari olarak temin edilebilen birçok heptan ürününde bulunmasına rağmen, heptan genellikle bir çözücü olarak kullanıldığından, büyük bir safsızlık olarak kabul edilmez. Bununla birlikte, damıtma ve rafine etme işlemleriyle 2-metilhekzanı n-heptan'dan ayırmak mümkündür.
Bir grup izomer içinde, daha fazla dalı olanlar daha kolay tutuşma ve daha tam yanma eğilimindedir. Bu nedenle, 2-metilhekzan, heptan ile karşılaştırıldığında daha düşük bir Kendiliğinden tutuşma sıcaklığına ve parlama noktasına sahiptir. Teorik olarak 2-metilhekzan daha az isli bir alevle yanar ve daha yüksek frekanslı radyasyon yayar; bununla birlikte, heptan ve 2-metilhekzan dallanma açısından sadece bir karbon atomu kadar farklılık gösterdiğinden, her ikisi de tutuşturulduğunda parlak sarı bir alevle yanar.
n-heptan ile karşılaştırıldığında, 2-metilhekzan ayrıca daha düşük erime ve kaynama noktalarına sahiptir. 2-Metilhekzanda heptan'dan daha düşük bir sıvı yoğunluğu bulunur.
NFPA 704 ölçeğinde, 2-metilhekzan, çeşitli diğer alkanlarla birlikte bir reaktivite seviyesi-0 kimyasal olarak listelenmiştir. Aslında, çoğu alkan, yanma veya güçlü güneş ışığı gibi ekstrem koşullar dışında reaktif değildir. Oksijen ve alevin varlığında, heptan gibi 2-metilhekzan, çoğunlukla tamamen su ve karbondiokside yanar. UV ışığı ile ve çözücüler içinde halojenlerle karıştırıldığında, genellikle 1,1,1-trikloroetan içinde brom, bir ikame reaksiyonu meydana getirir.
Ayrıca bakınız
değiştirKaynakça
değiştir- ^ "2-METHYLHEXANE - Compound Summary". PubChem Compound. Identification and Related Records: National Center for Biotechnology Information. 26 Mart 2005. 27 Mayıs 2015 tarihinde kaynağından arşivlendi. Erişim tarihi: 6 Mart 2012.
- "2-Methylhexane". chemexper.com. 4 Nisan 2012 tarihinde kaynağından arşivlendi. Erişim tarihi: 22 Kasım 2011.
- "Material Safety Data Sheet" (PDF). ChemADVISOR. 21 Mart 2006 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 22 Kasım 2011.
- "Isoheptane". INCHEM: Chemical Safety Information from Intergovernmental Organizations. International Programme on Chemical Safety. Ekim 2002. 28 Temmuz 2003 tarihinde kaynağından arşivlendi. Erişim tarihi: 22 Kasım 2011.
