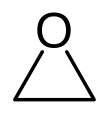
Etilen oksit
Etilen oksit veya oksiran (C2H4O), hafifçe tatlı kokusu olan renksiz, zehirli ve yanıcı bir gazdır. Halkalı bir eter ve en basit epoksittir: bir oksijen atomu ve iki karbon atomundan oluşan üç üyeli bir halkadır. Gerilmiş bir halka olduğu için etilen oksit, halka açılmasıyla sonuçlanan bir dizi katılma reaksiyonlarına kolayca katılır.
| |||
| Adlandırmalar | |||
|---|---|---|---|
| Tanımlayıcılar | |||
3D model (JSmol)
|
|||
| ECHA InfoCard | 100.000.773 | ||
| EC Numarası |
| ||
PubChem CID
|
|||
| RTECS numarası |
| ||
CompTox Bilgi Panosu (EPA)
|
|||
| |||
| |||
| Özellikler | |||
| Molekül formülü | C2H4O | ||
| Molekül kütlesi | 44.052 g/mol−1[2] | ||
| Görünüm | Renksiz gaz | ||
| Yoğunluk | 0.8821 g/cm3[2] | ||
| Erime noktası | −112.46 °C | ||
| Kaynama noktası | 10.4 °C | ||
| Tehlikeler | |||
| NFPA 704 (yangın karosu) |
|||
| Güvenlik bilgi formu (SDS) | External MSDS | ||
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa).
| |||
| Bilgi kutusu kaynakları | |||
Etilen oksit, asetaldehit ve vinil alkol ile izomerik olup endüstriyel olarak etilenin gümüş katalizör varlığında oksidasyonu ile üretilir.
Etilen oksitin tehlikelerinin çoğundan sorumlu olan reaktivitesi de onu faydalı kılar. Etilen oksit, doğrudan evde kullanım için çok tehlikeli ve tüketiciler için genellikle yabancı olmasına rağmen, pek çok tüketici ürününün yanı sıra tüketici dışı kimyasallar ve ara ürünler yapmak için kullanılır. Bu ürünler arasında deterjanlar, koyulaştırıcılar, solventler, plastikler ve etilen glikol, etanolaminler, basit ve kompleks glikoller, poliglikol eterler ve diğer bileşikler gibi çeşitli organik kimyasallar bulunur. Genellikle alternatif malzemelerden daha etkili ve daha az toksik olan polisorbat 20 ve polietilen glikol (PEG) gibi ürünlerin üretimi de dahil olmak üzere çeşitli uygulamaları olan hayati bir ham madde olmasına rağmen, etilen oksitin kendisi çok tehlikeli bir maddedir. Oda sıcaklığında çok yanıcı, kanserojen, mutajen, tahriş edici ve anestezik bir gazdır.[3]
Etilen oksit, hastanelerde ve tıbbi ekipman endüstrisinde, tek kullanımlık plastik şırıngalar gibi ısıya duyarlı alet ve ekipmanların sterilizasyonunda buharın yerini almak için yaygın olarak kullanılan bir yüzey dezenfektanıdır.[4]
Kaynakça
değiştir- ^ Oxirane | C2H4O – PubChem 2 Şubat 2014 tarihinde Wayback Machine sitesinde arşivlendi.. Pubchem.ncbi.nlm.nih.gov. 14 Ekim 2017 tarihinde erişilmiştir.
- ^ a b Haynes, p. 3.430
- ^ Rebsdat, Siegfried and Mayer, Dieter (2005) "Ethylene Oxide" in Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH, Weinheim.
- ^ McKetta, John J.; Cunningham, William A. (1984). Encyclopedia of Chemical Processing and Design. Vol. 20. CRC Press. p. 309. ISBN 0-8247-2470-4.
Konuyla ilgili yayınlar
değiştir- Haynes, William M. (2011). CRC Handbook of Chemistry and Physics. 92. Boca Raton, Florida: CRC Press. ISBN 1439855110.
Dış bağlantılar
değiştir- EOSA Promoting the safe use of Ethylene Oxide for Sterilization 25 Ekim 2020 tarihinde Wayback Machine sitesinde arşivlendi.
- WebBook page for C2H4O 15 Ekim 2017 tarihinde Wayback Machine sitesinde arşivlendi.
- National Institute for Occupational Safety and Health – Ethylene Oxide Topic Page 15 Ekim 2017 tarihinde Wayback Machine sitesinde arşivlendi.
- CDC – NIOSH Pocket Guide to Chemical Hazards 15 Ekim 2017 tarihinde Wayback Machine sitesinde arşivlendi.
- EOSA memo about Ethylene Oxide (EtO) facts 15 Ekim 2017 tarihinde Wayback Machine sitesinde arşivlendi.
| Kimya ile ilgili bu madde taslak seviyesindedir. Madde içeriğini genişleterek Vikipedi'ye katkı sağlayabilirsiniz. |