Sorbik asit
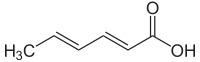
Sorbik asit veya 2,4-heksadienoik asit, gıda koruyucu olarak kullanılan doğal bir organik bileşik'tir.[1] CH3(CH)4CO2H kimyasal formülüne sahiptir. Suda az çözünür ve kolayca süblimleşir renksiz bir katıdır. İlk olarak “Sorbus aucuparia”nın (üvez ağacının olgunlaşmamış meyvelerinden yalıtıldığından onun adını almıştır.
| |

| |
| Adlandırmalar | |
|---|---|
Tercih edilen IUPAC adı (2E,4E)-Hexa-2,4-dienoic acid | |
| Tanımlayıcılar | |
3D model (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard | 100.003.427 |
| E numaraları | E200 (koruyucular) |
PubChem CID
|
|
| UNII | |
CompTox Bilgi Panosu (EPA)
|
|
| |
| |
| Özellikler | |
| Kimyasal formül | C6H8O2 |
| Molekül kütlesi | 112,13 g mol−1 |
| Yoğunluk | 1,204 g/cm3 |
| Erime noktası | 135 °C (275 °F; 408 K) |
| Kaynama noktası | 228 °C (442 °F; 501 K) |
| Çözünürlük (su içinde) | 1,6 g/L at 20 °C |
| Asitlik (pKa) | 4,76 at 25 °C |
| Tehlikeler | |
| NFPA 704 (yangın karosu) |
|
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa).
| |
| Bilgi kutusu kaynakları | |
Üretim değiştir
Sorbik aside giden geleneksel yol, malonik asit ve trans-bütenal'in yoğunlaştırılmasını kapsar.[2] Allil klorür, asetilen ve karbon monoksit'in nikel katalizli reaksiyonu yoluyla elde edilebilen izomerik heksadienoik asitlerden de hazırlanabilir. Ancak ticari olarak kullanılan yol krotonaldehit ve ketene'den üretimdir.[3] Yıllık tahmini 30,000 ton üretilir.[4]
Kaynakça değiştir
- ^ Piper JD, Piper PW (2017). "Benzoate and Sorbate Salts: A Systematic Review of the Potential Hazards of These Invaluable Preservatives and the Expanding Spectrum of Clinical Uses for Sodium Benzoate". Comprehensive Reviews in Food Science and Food Safety. 16 (5): 868-880. doi:10.1111/1541-4337.12284 . PMID 33371618.
- ^ C. F. H. Allen, J. VanAllan (1944). "Sorbic Acid". Org. Synth. 24: 92. doi:10.15227/orgsyn.024.0092.
- ^ Ashford's Dictionary of Industrial Chemicals, Third edition, 2011, page 8482
- ^ Erich Lück, Martin Jager and Nico Raczek "Sorbic Acid" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2000.DOI:10.1002/14356007.a24_507
