Kurşun(II) oksit
Kurşun monoksit olarak da adlandırılan kurşun(II) oksit, PbO moleküler formülüne sahip inorganik bileşiktir. PbO iki polimorfda oluşur: tetragonal kristal yapıya sahip litarj ve ortorombik kristal yapıya sahip massikot. PbO için modern uygulamalar çoğunlukla kurşun bazlı endüstriyel cam ve, bilgisayar bileşenlerini de kapsayan endüstriyel seramiklerdir. Amfoterik bir oksittir.[3]

| |
| |
| Adlandırmalar | |
|---|---|
Kurşun(II) oksit | |
| Tanımlayıcılar | |
| ChemSpider | |
| ECHA InfoCard | 100.013.880 |
PubChem CID
|
|
| RTECS numarası |
|
| UNII | |
| UN numarası | 3288 |
CompTox Bilgi Panosu (EPA)
|
|
| Özellikler | |
| Molekül formülü | PbO |
| Molekül kütlesi | 223.20 g/mol |
| Görünüm | kırmızı veya sarı toz |
| Yoğunluk | 9.53 g/cm3 |
| Erime noktası | 888 °C |
| Kaynama noktası | 1477 °C |
| Çözünürlük (su içinde) | 0.017 g/L[1] |
| Çözünürlük | seyreltik alkaliler, alkol’de çözünmez derişik alkalilerde çözünür HCl, amonyum klorür’de çözünür |
| 4,20×10-5 cm3/mol | |
| Yapı | |
| Tetragonal, tP4 | |
| Tehlikeler | |
| GHS etiketleme sistemi: | |
| Piktogramlar |   
|
| İşaret sözcüğü | Tehlike |
| R-ibareleri | R61, R20/22, R33, R62, R50/53 |
| G-ibareleri | S53, S45, S60, S61 |
| Tehlike ifadeleri | H302+H332, H351, H360Df, H362, H372, H410 |
| Önlem ifadeleri | P201, P260, P263, P280, P301+P312+P330, P308+P313 |
| NFPA 704 (yangın karosu) |
|
| Parlama noktası | Yanıcı değil |
| Öldürücü doz veya konsantrasyon (LD, LC): | |
LDLo (yayınlanan en düşük)
|
1400 mg/kg (köpek, oral)[2] |
| AB sınıflandırması | Repr. Cat. 1/3 Zehirli (T) Zararlı (Xn) Çevre için tehlikeli (N) |
| Güvenlik bilgi formu (SDS) | ICSC 0288 |
| Benzeyen bileşikler | |
Diğer anyonlar
|
Kurşun sülfür Kurşun selenid Kurşun tellürid |
Diğer katyonlar
|
Karbon monoksit Silisyum monoksit Kalay(II) oksit |
Benzeyen
|
Kurşun(II,IV) oksit Kurşun dioksit |
Benzeyen bileşikler
|
Talyum(III) oksit Bizmut(III) oksit |
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa).
| |
| Bilgi kutusu kaynakları | |
Yapımı değiştir
PbO, kurşun metalinin yaklaşık 600 °C’de havada ısıtılmasıyla hazırlanabilir . Bu sıcaklıkta, diğer kurşun oksitlerin havada oksidasyonunun da son ürünüdür:[4]
- PbO2 Pb12O19 Pb12O17 Pb3O4 PbO
Kurşun(II) nitrat veya kurşun(II) karbonatın termal ayrışması da PbO oluşumuna neden olur:
PbO, ham kurşun cevherlerini metalik kurşun haline getirmek için büyük bir ara ürün olarak üretilir. Kurşun cevheri çoğunlukla galendir (kurşun(II) sülfür). Yaklaşık 1000 °C sıcaklıkta sülfür, oksite dönüştürülür:[5]
- 2 PbS + 3 O2 → 2 PbO + 2 SO2
Metalik kurşun, PbO’in karbon monoksit ile yaklaşık 1200 °C’de indirgenmesiyle elde edilir:[6]
- PbO + CO → Pb + CO2
Yapısı değiştir
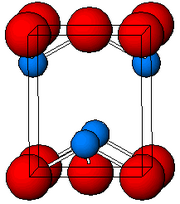
X ışını kristalografisi ile belirlendiği gibi, hem polimorflar hem de tetragonal ve ortorombik piramidal dört koordinatlı bir kurşun merkeze sahiptir. Tetragonal formda dört kurşun–oksijen bağı aynı uzunluğa sahiptir. Ancak, ortorombikte bağların ikisi daha kısa ve ikisi daha uzundur. Piramidal görünüş stereokimyasal olarak aktif yalın çift elektron varlığını gösterir.[7] PbO, tetragonal örgü yapısında meydana geldiğinde buna litarj; ve PbO, ortorombik örgü yapısına sahip olduğunda buna massikot denir. PbO kontrollü ısıtma ve soğutma ile massikottan litarja veya tersi olarak değiştirilebilir.[8] Tetragonal form genellikle kırmızı veya turuncu, ortorombik formda genellikle sarı veya turuncudur. Ancak, renk yapının çok güvenilir bir göstergesi değildir.[9] PbO’in tetragonal ve ortorombik formları doğal olarak nadir mineraller olarak bulunur.
Reaksiyonları değiştir
Bu maddenin kırmızı ve sarı formları entalpideki küçük bir değişikle ilişkilidir:
- PbO(kırmızı) → PbO(sarı) ΔH = 1.6 kJ/mol
PbO amfoteriktir, yani hem asitlerle hem de bazlarla reaksiyona girer. Asitlerle, [Pb6O(OH)6]+4 gibi okso kümelerinin aracılığıyla Pb+2 tuzları oluşturur. Kuvvetli bazlarla, PbO plumbit (plumbat(II) olarak da adlandırılır) tuzları oluşturmak için çözünür:[10]
- PbO + H2O + OH− → [Pb(OH)]−3
Uygulama alanları değiştir
Kurşun camdaki kurşun türü normalde PbO’dir. Bu nedenle, PbO cam yapımında yaygın olarak kullanılır. Cama bağlı olarak, camda PbO kullanmanın faydası camın kırılma indisini arttırmak, camın viskozitesini azaltmak, camın elektriksel özdirencini arttırmak ve camın X ışınlarını absorbe etme kabiliyetini arttırmak gibi bir veya daha fazla olabilir. PbO’in endüstriyel seramiklere eklenmesi (camda olduğu gibi), malzemeleri manyetik ve elektriksel olarak daha inert hâle getirir (Curie sıcaklığını arttırarak) ve genelliklede bu amaçla kullanılır.[11] Tarihsel olarak PbO, ev seramikleri için seramik sırlarında da yaygın olarak kullanılmıştır ve hâlen kullanılmaktadır, ancak artık yaygın olarak kullanılmamaktadır. Diğer daha az baskın uygulamalar, kauçuğun vulkanizasyonu ve belirli pigmentlerin ve boyaların üretimini içerir.[3] PbO, katot ışını tüpünün camında X ışını emisyonunu engellemek için kullanılır, ancak esas olarak boyun ve hunide kullanılır çünkü ön panelde kullanıldığında renk değişikliğine neden olabilir. Ön panel için stronsiyum oksit tercih edilir.
Kurşun tüketimi ve dolayısıyla PbO'nun işlenmesi otomobil sayısı ile ilişkilidir, çünkü otomobil kurşun asit akülerinin ana bileşeni olmaya devam etmektedir.[12]
Özelleşmiş veya azalan kullanımlar değiştir
Sert, su geçirmez bir çimento oluşturacak şekilde gliserin ile PbO karışımı, akvaryumların düz cam yanlarını ve tabanlarını birleştirmek için ve ayrıca bir zamanlar pencere çerçevelerindeki cam panellerin yalıtımı için kullanılmıştır. Kurşun boyaların bir bileşenidir.
PbO, bir tür Çin konserve yumurtası olan yüzyıl yumurtalarının kalitesini yapay olarak arttırmak ve daha kısa sürede daha fazla kar elde etme sürecini hızlandırmak için kullanıldı. Bu, bazı küçük fabrikalarda vicdansız bir uygulamaydı, ancak Çin'de yaygınlaştı ve skandal 2013'te yaygınlaştıktan sonra birçok dürüst üreticiyi kutularına "kurşunsuz" olarak etiket basmaya zorladı.
Toz halinde litarj formunda, yaldız yapımında kullanılan hava şartlarına dayanıklı bir haşıl oluşturmak için bezir yağı ile karıştırılıp kaynatılabilir. Litarj, altın varağa sıcak ve parlak görünmesini sağlayan koyu kırmızı bir renk verirken, bezir yağı yapışma ve dayanıklı düz bir ciltleme yüzeyi sağlar.
PbO organik sentezde, belirli kondenzasyon reaksiyonlarında kullanılır.[13]
PbO, Plumbikon adı verilen bir video kamera tüpündeki giriş fotoiletkenidir.
Sağlık sorunları değiştir
Kurşun oksit solunduğunda veya yutulduğunda ölümcül olabilir. Deride, gözlerde ve solunum yolunda tahrişe neden olur. Diş eti dokusunu, merkezî sinir sistemini, böbrekleri, kanı ve üreme sistemini etkiler. Bitkilerde ve memelilerde biyolojik birikmeye uğrayabilir.[14]
Kaynakça değiştir
- ^ Blei(II)-oxid[ölü/kırık bağlantı]. Merck
- ^ "Kurşun bileşikleri (Pb olarak)". Immediately Dangerous to Life or Health Concentrations (IDLH). Ulusal İş Sağlığı ve Güvenliği Enstitüsü (NIOSH).
- ^ a b Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a15_249.
- ^ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2. bas.). Butterworth-Heinemann. ISBN 0080379419.[sayfa belirt]
- ^ Abdel-Rehim, A. M. (2006). "Thermal and XRD analysis of Egyptian galena". Journal of Thermal Analysis and Calorimetry. 86 (2): 393-401. doi:10.1007/s10973-005-6785-6.
- ^ Lead Processing @ Universalium.academic.ru 24 Temmuz 2020 tarihinde Wayback Machine sitesinde arşivlendi.. Alt address: Lead processing @ Enwiki.net 22 Şubat 2017 tarihinde Wayback Machine sitesinde arşivlendi..
- ^ Şablon:Wells5th[sayfa belirt]
- ^ A simple example is given in Anil Kumar De (2007). "§9.2.6 Lead (Pb): Lead Monoxide PbO". A Textbook Of Inorganic Chemistry. New Age International. s. 383. ISBN 978-81-224-1384-7. A more complex example is in Turova, N.Y. (2002). "§9.4 Germanium, tin, lead alkoxides". The Chemistry of Metal Alkoxides. Springer. s. 115. ISBN 978-0-7923-7521-0. 16 Ocak 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 7 Ağustos 2020.
- ^ Rowe, David John (1983). Lead Manufacturing in Britain: A History. Croom Helm. s. 16. ISBN 978-0-7099-2250-6.
- ^ Şablon:Holleman&Wiberg[sayfa belirt]
- ^ Chapter 9, "Lead Compounds", in the book Ceramic and Glass Materials: Structure, Properties and Processing 2 Aralık 2017 tarihinde Wayback Machine sitesinde arşivlendi., published by Springer, year 2008.
- ^ Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a15_193.pub2.
- ^ "Organic Syntheses". Organic Syntheses.; Collective Volume, 2, s. 229
- ^ "Lead(II) oxide". International Occupational Safety and Health Information Centre. 15 Aralık 2011 tarihinde kaynağından arşivlendi. Erişim tarihi: 6 Haziran 2009.
Dış bağlantılar değiştir
- Case Studies in Environmental Medicine - Lead Toxicity5 Haziran 2009 tarihinde Wayback Machine sitesinde arşivlendi.
- ToxFAQs: Lead4 Şubat 2016 tarihinde Wayback Machine sitesinde arşivlendi.
- National Pollutant Inventory - Lead and Lead Compounds Fact Sheet
- Webelements PbO 27 Temmuz 2020 tarihinde Wayback Machine sitesinde arşivlendi.
