Enantiyoselektif sentez
Enantiyoselektif sentez ya da asimetrik sentez, [1] bir kimyasal sentez şeklidir. IUPAC, bir veya daha fazla yeni kiralite elementinin bir substrat molekülünde oluşturulduğu ve stereoizomerik (enantiyomerik veya diastereoizomerik) ürünleri eşit olmayan miktarlarda üreten kimyasal reaksiyon (veya reaksiyon sekansı) olarak tanımlanır.[2]
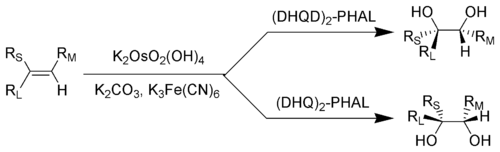
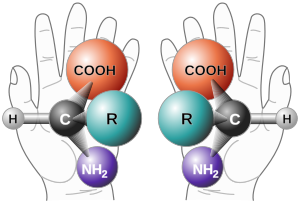
Daha açık bir ifadeyle: bir bileşiğin, belirli bir enantiyomer veya diastereomer oluşumunu destekleyen bir yöntemle sentezidir.
Enantiyoselektif sentez, modern kimyada kilit bir işlemdir ve bir molekülün farklı enantiyomerlerinin veya diastereomerlerinin çoğu zaman farklı biyolojik aktiviteye sahip olması nedeniyle farmasötikler alanında özellikle önemlidir.
Genel bakış değiştir
Şeker ve amino asitler gibi biyolojik sistemlerin yapı taşlarının birçoğu yalnızca bir enantiyomer olarak üretilir. Sonuç olarak, canlı sistemler yüksek derecede kimyasal kiralılığa sahiptir ve genellikle belirli bir bileşiğin çeşitli enantiyomerleriyle farklı şekilde reaksiyona girer. Bu seçiciliğe örnekler:
- Lezzet: yapay tatlandırıcı aspartamın iki enantiyomeri vardır. L- aspartam tatlıdır, D- aspartam tatsızdır.[3]
- Koku: R - (-) - carvon nane gibi kokarken, S - (+) - carvone kimyon gibi kokar.[4]
- İlaç etkinliği: antidepresan ilaç olan Citalopram rasemik bir karışım halinde satılmaktadır. Bununla birlikte, çalışmalar ilacın faydalı etkilerinden sadece (S) - (+) enantiyomerinin sorumlu olduğunu göstermiştir.[5][6]
- İlaç güvenliği: D-penisilamin şelasyon tedavisinde ve romatoid artrit tedavisinde kullanılırken, L‑penisilamin, temel bir B vitamini olan piridoksinin etkisini engellediği için toksiktir.[7]
Bu enantiyoselektif sentezin büyük önemi olduğundan, elde edilmesi de zor olabilir. Enantiyomerler, aynı entalpi ve entropilere sahiptir ve bu nedenle, rasemik bir karışıma yol açan, yönlendirilmemiş bir işlemle eşit miktarlarda üretilmelidir. Enantiyoselektif sentez, geçiş durumundaki etkileşimler yoluyla bir enantiyomerin bir diğerinin üzerinde oluşumunu destekleyen kiral bir özellik kullanılarak elde edilebilir. Bu önyargı asimetrik indüksiyon olarak bilinir ve substrat, reaktif, katalizör veya ortamdaki kiral özellikleri içerebilir [8] ve bir enantiyomeri oluşturmak için gereken aktivasyon enerjisini karşıt enantiyomerinkinden daha düşük hale getirerek çalışır.[9]
Enantioselektivite genellikle, bir enantiyomer farklılaştırıcı basamağın nispi oranları ile belirlenir - bir reaktifin iki enantiyomerik üründen biri olabileceği nokta. Bir reaksiyon için hız sabiti, k, reaksiyonun aktivasyon enerjisinin bir fonksiyonudur, bazen enerji engeli olarak adlandırılır ve sıcaklığa bağlıdır. Enerji bariyerinin Gibbs serbest enerjisini kullanarak, ΔG *, belirli bir sıcaklıkta, T, karşılıklı stereokimyasal sonuçların oranları:
Sıcaklık farklılığı oran farklılığı anlamına gelir, böylece enantiyoselektivite düşük sıcaklarda daha da büyük olarak gözlemlenir. Sonuç olarak, küçük enerji-bariyer farklılıkları bile gözle görülür bir etkiye neden olabilir.
Yaklaşımlar değiştir
Enantiyoselektif kataliz değiştir
Genel olarak, enantiyoselektif kataliz (geleneksel olarak asimetrik kataliz olarak bilinir), kiral koordinasyon kompleksleridir. Kataliz, diğer enantioselektif sentez yöntemlerinden daha geniş bir dönüşüm aralığı için etkilidir. Katalizörler, kiral ligandlar kullanılarak neredeyse hiç değişmez şekilde kiral hale getirilirler (ayrıca, daha basit akiral ligandlar kullanılarak metal-kiral-metal kompleksleri üretmek de mümkündür, ancak bu tür türlerin nadiren sentetik olarak faydalı olduğu kanıtlanmıştır).[10] Çoğu enantiyoselektif katalizör, düşük substrat/katalizör oranlarında etkilidir.[11][12] Yüksek verimleri göz önüne alındığında, pahalı katalizörlerde bile endüstriyel skala sentezi için genellikle uygundurlar.[13] Çok yönlü bir enantioselektif sentez örneği, çok çeşitli fonksiyonel grupları azaltmak için kullanılan asimetrik hidrojenasyondur.
| ΔΔG* (kcal) | 273 K'de k1/k2 | 298 K'de k1/k2 | 323 K'de k1/k2 |
|---|---|---|---|
| 1.0 | 6.37 | 5.46 | 4.78 |
| 2.0 | 40.6 | 29.8 | 22.9 |
| 3.0 | 259 | 162 | 109 |
| 4.0 | 1650 | 886 | 524 |
| 5.0 | 10500 | 4830 | 2510 |
Yeni katalizörlerin tasarımına, yeni ligand sınıflarının gelişmesi büyük ölçüde egemendir. Genellikle 'imtiyazlı ligandlar' olarak adlandırılan bazı ligandların geniş bir reaksiyon aralığında etkili olduğu bulunmuştur; örnekler arasında BINOL, Salen ve BOX bulunur. Bununla birlikte, genel olarak, birkaç katalizör, birden fazla asimetrik reaksiyon tipinde etkilidir. Örneğin, BINAP/Ru ile Noyori asimetrik hidrojenasyonu, bir β-keton gerektirir, bununla birlikte başka bir katalizör olan BINAP/diamine-Ru, kapsamı a, alkenler ve aromatik kimyasallara genişletir.
Kiral yardımcılar değiştir
Bir kiral yardımcı, daha sonra intramoleküler asimetrik indüksiyon yoluyla enantioselektif reaksiyonlara girebilen yeni bir bileşik oluşturmak için başlangıç malzemesine bağlanan organik bir bileşiktir.[14][15] Reaksiyonun sonunda yardımcı ürünün rasemizasyonuna neden olmayacak koşullar altında uzaklaştırılır.[16] Genellikle daha sonra kullanmak üzere kurtarılır.
Kiral yardımcı maddeler, etkili olmak için stokiyometrik miktarlarda kullanılmalı ve yardımcı maddenin eklenmesi ve çıkarılması için ilave sentetik adımlar gerektirmelidir. Bununla birlikte, bazı durumlarda, mevcut tek stereoselektif metodoloji, kiral yardımcılara dayanır ve bu reaksiyonlar, enantiyomerik açıdan saf ürünlere en zaman verimli erişim sağlayan, çok yönlü ve çok iyi çalışılmış olma eğilimindedir.[15] Ek olarak, yardımcı yönelimli reaksiyonların ürünleri, kolon kromatografisi veya kristalizasyon gibi yöntemlerle kolay ayrılmalarını sağlayan diastereomerlerdir .
Biyokataliz değiştir
Biyokataliz, izole edilmiş enzimlerden canlı hücrelere kadar değişen biyolojik bileşikleri kimyasal dönüşümler yapmak için kullanır.[17][18] Bu reaktiflerin avantajları, çok yüksek e.e.s ve reaktif spesifikliğinin yanı sıra, hafif çalışma koşulları ve düşük çevresel etki içerir. Biyokatalizörler, endüstride akademik araştırmalardan daha yaygın olarak kullanılmaktadır;[19] örneğin statinlerin üretiminde.[20] Bununla birlikte, yüksek reaktif spesifikliği, etkili bir reaktif bulunmadan önce çok çeşitli biyokatalizörlerin taranmasını gerektirdiği için bir problem olabilir.
Enantiyoselektif organokataliz değiştir
Organokataliz, kimyasal reaksiyon hızının karbon, hidrojen, kükürt ve diğer metal olmayan elementlerden oluşan organik bir bileşik ile arttırıldığı bir kataliz formunu belirtir.[21][22] Organocatalyst, kiral olduğunda enantioselektif sentez elde edilebilir;[23][24] örneğin bir dizi karbon-karbon bağı oluşturucu reaksiyon, prolin varlığında enantiyoselektif hale gelmiştir, en iyi örnek aldol reaksiyonudur.[25] Organokataliz genellikle kiral katalizörler olarak doğal bileşikler ve ikincil aminler kullanır;[26] bunlar metal içermemesi nedeniyle ucuz ve çevre dostudur.
Kiral havuz sentezi değiştir
Kiral havuzu sentezi, enantioselektif sentez için en basit ve en eski yaklaşımlardan biridir. Kolayca temin edilebilen bir kiral başlangıç materyali, istenen hedef molekülü elde etmek için, çoğunlukla akiral reaktifler kullanılarak, ardışık reaksiyonlar vasıtasıyla manipüle edilir. SN2 reaksiyonunda olduğu gibi yeni kiral türler oluşturulduğunda, enantiyoselektif sentez için kriterleri karşılayabilmektedir.
Kiral havuzu sentezi, şeker veya amino asit gibi nispeten ucuz doğal olarak oluşan bir yapı bloğuna benzer kiraliteye sahip hedef moleküller için özellikle çekicidir. Bununla birlikte, molekülün maruz kalabileceği olası reaksiyonların sayısı sınırlıdır ve kıvrımlı sentetik yollar gerekli olabilir (örn. Oseltamivir toplam sentezi). Bu yaklaşım aynı zamanda, eğer doğal olarak oluşmazsa pahalı olabilecek enantiyopur başlangıç malzemesinin stokiyometrik miktarını gerektirir.
Alternatif yaklaşımlar değiştir
Enantiyoselektif senteze alternatifler, genellikle bir enantiyomerin rasemik bir karışımdan, birkaç yöntemden herhangi biri ile izole edilmesini içerir. Bu tür rasemik karışımları yapmak için gereken zaman ve maliyet düşükse (veya her iki enantiyomerin de kullanım alanı bulunabilirse), bu yaklaşım düşük maliyetli kalabilir. Yaygın ayırma yöntemleri, kiral çözünürlük veya kinetik çözünürlüğe dayanır.
Enantiyomerlerin ayrılması ve analizi değiştir
Bir molekülün iki enantiyomeri, aynı fiziksel özelliklere (erime noktası, kaynama noktası, polarite, vb.) sahiptir ve bu nedenle birbirleriyle aynı şekilde davranırlar. Sonuç olarak, ince tabaka kromatografisinde aynı Rf ile göç edecekler ve HPLC ve GC'de aynı alıkonma sürelerine sahip olacaklardır. NMR ve IR spektrumları aynıdır.
Bu, bir işlemin tek bir enantiyomer üretip üretmediğini (ve en önemlisi hangi enantiyomer olduğunu) belirlemeyi zorlaştırabilir ve ayrıca enantiyomerleri %100 enantiyoselektif olmayan bir reaksiyondan ayırmayı zorlaştırır. Neyse ki, enantiyomerler diğer kiral materyallerin varlığında farklı davranırlar ve bunların ayrılma ve analizine izin vermek için kullanılabilir.
Enantiyomerler, kuvars veya kiral olarak değiştirilmiş standart ortamlar gibi kiral kromatografik ortamlar üzerinde aynı şekilde göç etmezler. Bu, GC ve HPLC yoluyla analize izin vermek için küçük bir ölçekte veya kiral olarak saf olmayan maddeleri ayırmak için büyük bir ölçekte kullanılabilen kiral kolon kromatografisinin temelini oluşturur. Bununla birlikte, bu işlem pahalı olabilecek büyük miktarda kiral paketleme malzemesi gerektirebilir. Yaygın bir alternatif, enantiyomerleri, kiral yardımcı maddelerle aynı şekilde bir diyastereomerlere dönüştürmek için bir kiral türevlendirme maddesinin kullanılmasıdır. Bunlar farklı fiziksel özelliklere sahiptir ve bu nedenle geleneksel yöntemler kullanılarak ayrılabilir ve analiz edilebilir. 'Kiral çözünürlük ajanları' olarak bilinen özel kiral türevlendirme ajanları, stereoizomerlerin NMR spektroskopisinde kullanılır, bunlar tipik olarak Eu(fod)3 ve Eu(hfc)3 gibi kiral europium komplekslerinin koordinasyonunu içerir.
Bir maddenin enantiyomerik fazlalığı ayrıca bazı optik yöntemler kullanılarak belirlenebilir. Bunu yapmak için en eski yöntem, üründeki optik dönme seviyesini bilinen bir bileşimin standartına göre karşılaştırmak için bir polarimetre kullanmaktır. Pamuk etkisinden yararlanarak stereoizomerlerin ultraviyole görünür spektroskopisini yapmak da mümkündür.
Bileşiğin kiralitesini belirlemenin en doğru yollarından biri, X-ışını kristalografisi ile mutlak konfigürasyonunu belirlemektir. Ancak bu, uygun bir tek kristalin yetiştirilmesini gerektiren emek yoğun bir işlemdir.
Tarihçe değiştir
Başlangıç (1815-1905) değiştir
1815'te Fransız fizikçi Jean-Baptiste Biot, bazı kimyasalların optik aktivite denilen bir özellik olan polarize ışık demetinin düzlemini döndürebileceğini gösterdi.[27] Bu özellik doğası 1848'de Louis Pasteur, bu "simetrik olmayan" biçimin moleküler dayanağa sahip olması gerektiğini önerene kadar bir sır olarak kalmıştır.[28][29] Bir yıl sonra Lord Kelvin tarafından icat edilen kiralite tabiri ile birlikte anılmaya başlanmıştır.[30] Kirallik orijini, nihayet 1874’de, Jacobus Henricus van't Hoff ve Joseph Le Bel'in bağımsız olarak karbonun tetrahedral geometrisini önermesiyle tanımlandı.[31][32] Bu çalışma öncesi yapısal modeller iki boyutlu olmuştu ve van't Hoff ve Le Bel, bu tetrahedronun etrafındaki grupların düzenlenişinin bileşiğin optik aktivitesini belirleyebileceğini teorik olarak ortaya koydu. Bugün bu kuralı Le Bel-van 't Hoff kuralı olarak biliyoruz .
1894'te Hermann Emil Fischer asimetrik indüksiyon kavramını ana hatlarıyla açıkladı;[34] seçici olarak, klorofil içindeki optik olarak aktif maddelerin etkisinden dolayı, bitkiler tarafından D- glikoz oluşumunu doğru şekilde seçtiğini belirtti. Fischer aynı zamanda, enantiyoselektif sentezin ilk örneği olacak bir işlemle şekerleri enantiyoselektif olarak uzatarak, bugün Kiliani-Fischer sentezi olarak kabul edilen sentezi başarıyla gerçekleştirmiştir.[35]
İlk enantioselektif kimyasal sentez, 2-etil-2-metil malonik asidin bir brusin-katalize edilmiş enantioselektif dekarboksilasyonu için, Willy Marckwald, Universität zu Berlin'e atfedilir.[33][36] 2-metilbütirik asit reaksiyon ürününün levorotar formunun biraz fazlası üretildi; bu ürün aynı zamanda doğal bir üründür - örneğin, biyosentezi sırasında diketit sentazının (LovF) oluşturduğu bir lovastatinin bir yan zinciri olarak oluşur [37] - bu sonuç, enantiyoselektivite ile kaydedilen ilk toplam sentezi oluşturur. İmza attığı diğer ilkler, Koskinen'in belirttiği üzere "asimetrik kataliz , enantiotopik seleksiyon ve organokatalizin ilk örneği"dir.[33] Enantiyoselektif sentez, sadece yaşamsallık anlamında anlaşılabildiği için, bu gözlem tarihi öneme sahiptir. Jöns Jacob Berzelius gibi birçok önde gelen kimyager o zamanlar doğal ve yapay bileşiklerin temelde farklı olduğunu ve kiralilitenin sadece doğal bileşiklerde var olabilecek “hayati kuvvetin” bir tezahürü olduğunu savundu.[38] Fischer'den farklı olarak, Marckwald, bir kiral organokatalyör ile de olsa (şimdi bu kimyayı anladığımız gibi), bir aviral, doğal olmayan başlangıç materyali üzerine enantioselektif bir reaksiyon gerçekleştirmiştir.[33][39][40]
Erken çalışmalar (1905–1965) değiştir
Enantiyoselektif sentezin gelişimi, büyük ölçüde, ayırma ve analiz için mevcut olan sınırlı teknik yelpazesi nedeniyle, yavaştı. Diastereomerler, geleneksel yollarla ayrılmaya izin veren farklı fiziksel özelliklere sahiptir, ancak o sırada enantiyomerler sadece kendiliğinden çözünürlükle (kristalleşme üzerine ayrılan enantiyomerlerin) veya kinetik çözünürlükle (bir enantiyomerin seçici olarak yok edildiği) ayrılabilir. Enantiyomerlerin analizi için tek araç, yapısal veri sağlamayan bir yöntem olan polarimetre kullanan optik aktivite idi.
1950'lere kadar büyük ilerleme gerçekten başlamamıştı. Kısmen RB Woodward ve Vladimir Prelog gibi kimyagerler tarafından ve aynı zamanda yeni tekniklerin geliştirilmesiyle yönlendirildi. Bunlardan ilki, 1951'de Johannes Bijvoet tarafından bir organik bileşiğin mutlak konfigürasyonunu belirlemek için kullanılan X-ışını kristalografisi idi.[41] Kiral kromatografi, bir yıl sonra kiral amino asitleri ayırmak için kağıt kromatografisini kullanan Dalgliesh tarafından tanıtıldı.[42] Her ne kadar bu tür ayrılmaları ilk gözlemleyen Dalgliesh olmasa da, enantiomerlerin ayrılmasını kiral selülozun diferansiyel tutulmasına doğru bir şekilde bağladı. Bu, Klem ve Reed'in ilk önce kiral HPLC ayrılması için kiral olarak modifiye edilmiş silika jel kullanıldığını bildirdiği 1960'ta genişletildi.[43]
Solda: (S) - talidomit
Sağ: (R) - talidomit
Talidomit değiştir
Farklı enantiyomerlere sahip bir ilacın farklı etkilere sebep olabileceği o dönemde Arthur Robertson Cushny'nin çalışmaları sayesinde bilinse de,[44][45] bu erken ilaç tasarımında ve testinde sorumluğu getirmiyordu. Bununla birlikte, talidomidin felaketinin ardından ilaçların gelişimi ve ruhsatlandırması çarpıcı biçimde değişti.
İlk olarak 1953'te sentezlenen talidomit,1957'den 1962'ye kadar sabah bulantısı için yaygın olarak reçete edildi, ancak kısa sürede ciddi şekilde teratojenik olduğu bulundu,[46] sonuçta 10.000'den fazla bebekte doğum kusurlarına yol açtı. Afet birçok ülkeyi Kefauver-Harris Değişikliği (ABD) ve 65/65 / EEC1 (AB) Direktifi gibi ilaçların test edilmesi ve ruhsatlandırılması için daha sert kurallar koymaya teşvik etti.
Fareler kullanılarak teratojenik mekanizma üzerine yapılan erken araştırmalar, bir talidomit enantiyomerinin teratojenik olduğunu, diğerinin ise tüm terapötik aktiviteye sahip olduğunu gösterdi. Bu teori daha sonra yanlış olarak gösterildi ve yenilendi. Bununla birlikte, ilaç tasarımında kiralitenin önemi artmış ve enantiyoselektif sentez araştırmalarının artması sağlanmıştır.
Modern çağ (1965'ten beri) değiştir
Cahn-Ingold – Prelog öncelik kuralları (genellikle CIP sistemi olarak kısaltılır) ilk kez 1966'da yayınlandı ve enantiyomerlerin daha kolay ve doğru bir şekilde tarif edilmesini sağlamadı.[47][48] Aynı yıl, gaz kromatografisi [49] ilk başarılı enantiyomerik ayrılmayı sağladı, bu teknolojinin o dönemde yaygın olarak kullanılması sebebiyle önemli bir gelişmeydi.
Metal katalizli enantioselektif sentezin, William S. Knowles, Ryōji Noyori ve K. Barry Sharpless tarafından önü açıldı; bunun için 2001'de Nobel Kimya Ödülü'nü alacaklardı. Knowles ve Noyori, 1968'de bağımsız olarak geliştirdikleri asimetrik hidrojenasyonun gelişmesiyle başladı. Knowles, Wilkinson'ın katalizöründeki akiral trifenilfosfin ligandlarını kiral fosfin ligandlarla değiştirdi. Bu deneysel katalizör, en az% 15 enantiyomerik fazlalığı olan asimetrik bir hidrojenasyonda kullanıldı. Endüstriyel ölçekli senteze enantiyoselektif metal katalizi uygulayan ilk kişi Knowles idi; Monsanto Şirketi için çalışırken, DIPAMP ligandını kullanarak L-DOPA üretimi için enantiyoselektif bir hidrojenasyon adımı geliştirdi.[50][51][52]
| Knowles: Asimetrik hidrojenasyon (1968) | Noyori: Enantiyoselektif siklopropanasyon (1968) |
|---|
Noyori, stiren metal-karbenoid siklopropanasyonu için kullandığı kiral bir Schiff baz ligandı kullanarak bir bakır kompleksi geliştirdi.[53] Knowles'in bulgularıyla ortak olarak, Noyori'nin bu birinci nesil ligand için enantiyomerik fazlalığa ilişkin sonuçları hayal kırıklığı yarattı: %6. Ancak devam eden araştırmalar sonunda Noyori asimetrik hidrojenasyon reaksiyonunun gelişmesine yol açtı.
Sharpless, 1970'lerde ve 1980'lerde asimetrik oksidasyonlar (Sharpless epoksidasyon,[54] Sharpless asimetrik dihidroksilasyon,[55] Sharpless oksiaminasyon [56] ) geliştirerek bu indirgeme reaksiyonlarını tamamlamıştır. Asimetrik oksiaminasyon reaksiyonu ile, osmium tetroksit kullanarak, en erken yapandır.
Aynı dönemde, kiral bileşiklerin NMR ile analizine izin verecek yöntemler geliştirilmiştir; Mosher asidi [57] gibi kiral türevlendirme ajanları veya ilk olarak Eu(DPM)3 gibi europium bazlı kaydırma reaktifleri kullanılarak.[58]
Kiral yardımcılar, EJ Corey tarafından 1978'de [59] tanıtıldı ve Dieter Enders'in çalışmalarında belirgin bir şekilde öne çıktılar. Aynı zamanda, Hajos – Parrish – Eder – Sauer – Wiechert reaksiyonunu içeren öncü çalışmalarla enantiyoselektif organokataliz geliştirildi. Enzim-katalizli enantiyoselektif reaksiyonlar 1980'lerde,[60] domuz karaciğeri esterazla asimetrik ester hidrolizi gibi uygulamalarıyla özellikle sanayide [61] de dahil olmak üzere daha yaygın olmuştur. Gelişen genetik mühendisliği teknolojisi, artan seçici selektif dönüşümlere izin vererek, enzimlerin spesifik işlemlere uyarlanmasına izin vermiştir. Örneğin, statin öncüllerinin asimetrik hidrojenasyonu.[15]
Ayrıca bakınız değiştir
- Aza-Baylis-Hillman reaksiyonu, enantiyoselektif sentezde kiral bir iyonik sıvı kullanımı için.
- Spontan mutlak asimetrik sentez, optik olarak aktif katalizörler veya yardımcı maddeler kullanılmadan kiral ürünlerin akiral öncüllerinden sentezi. Tabiattaki homokiralite tartışılması ile ilgilidir .
- Ataktik, enantiyoselektif sentezden kaynaklanan bir polimer özelliği.
Kaynakça değiştir
- ^ IUPAC, Compendium of Chemical Terminology, 2. basım (the "Gold Book") (1997). Düzeltilmiş çevrimiçi sürümü: (2006-) "asymmetric synthesis".
- ^ IUPAC, Compendium of Chemical Terminology, 2. basım (the "Gold Book") (1997). Düzeltilmiş çevrimiçi sürümü: (2006-) "stereoselective synthesis".
- ^ Gal, Joseph (2012). "The Discovery of Stereoselectivity at Biological Receptors: Arnaldo Piutti and the Taste of the Asparagine Enantiomers-History and Analysis on the 125th Anniversary". Chirality. 24 (12): 959–976. doi:10.1002/chir.22071PMID 23034823
- ^ Theodore J. Leitereg; Dante G. Guadagni; Jean Harris; Thomas R. Mon; Roy Teranishi (1971). "Chemical and sensory data supporting the difference between the odors of the enantiomeric carvones". J. Agric. Food Chem. 19 (4): 785–787. doi:10.1021/jf60176a035
- ^ Lepola U, Wade A, Andersen HF (May 2004). "Do equivalent doses of escitalopram and citalopram have similar efficacy? A pooled analysis of two positive placebo-controlled studies in major depressive disorder". Int Clin Psychopharmacol. 19 (3): 149–55. doi:10.1097/01.yic.0000122862.35081.cd PMID 15107657
- ^ Hyttel, J.; Bøgesø, K. P.; Perregaard, J.; Sánchez, C. (1992). "The pharmacological effect of citalopram resides in the (S)-(+)-enantiomer". Journal of Neural Transmission. 88 (2): 157–160. doi:10.1007/BF01244820 25 Şubat 2019 tarihinde Wayback Machine sitesinde arşivlendi. PMID 1632943
- ^ JAFFE, IA; ALTMAN, K; MERRYMAN, P (Oct 1964). "The Antipyridoxine Effect of Penicillamine in Man" The Journal of Clinical Investigation. 43: 1869–73. doi:10.1172/JCI105060 24 Şubat 2019 tarihinde Wayback Machine sitesinde arşivlendi. PMC 289631 24 Şubat 2019 tarihinde Wayback Machine sitesinde arşivlendi. PMID 14236210
- ^ IUPAC, Compendium of Chemical Terminology, 2. basım (the "Gold Book") (1997). Düzeltilmiş çevrimiçi sürümü: (2006-) "asymmetric induction".
- ^ Clayden, Jonathan; Greeves, Nick; Warren, Stuart; Wothers, Peter; (2001). Organic Chemistry (1st ed.). Oxford University Press. ISBN 978-0-19-850346-0 Page 1226
- ^ Bauer, Eike B. (2012). "Chiral-at-metal complexes and their catalytic applications in organic synthesis". Chemical Society Reviews (İngilizce). 41 (8). ss. 3153-67. doi:10.1039/C2CS15234G. PMID 22306968.
- ^ Jacobsen, Eric; Pfaltz, Andreas; Yamamoto, Hisashi (1999). Comprehensive asymmetric catalysis 1-3. Berlin: Springer. ISBN 9783540643371
- ^ M. Heitbaum; F. Glorius; I. Escher (2006). "Asymmetric Heterogeneous Catalysis". Angewandte Chemie International Edition.45 (29): 4732–4762. doi:10.1002/anie.200504212 PMID 16802397
- ^ Endüstri Ölçeğinde Asimetrik Kataliz, (Blaser, Schmidt), Wiley-VCH, 2004.
- ^ Roos, Gregory (2002). Compendium of chiral auxiliary applications. San Diego, CA: Acad. Press. ISBN 9780125953443
- ^ a b c Glorius, F.; Gnas, Y. (2006). "Chiral Auxiliaries – Principles and Recent Applications".Synthesis. 2006 (12): 1899–1930. doi:10.1055/s-2006-942399 Kaynak hatası: Geçersiz
<ref>etiketi: "Glorius review" adı farklı içerikte birden fazla tanımlanmış (Bkz: Kaynak gösterme) - ^ Evans, D. A.; Helmchen, G.; Rüping, M. (2007). "Chiral Auxiliaries in Asymmetric Synthesis". In Christmann, M. Asymmetric Synthesis – The Essentials. Wiley-VCH Verlag GmbH & Co. pp. 3–9. ISBN 978-3-527-31399-0.
- ^ IUPAC, Compendium of Chemical Terminology, 2. basım (the "Gold Book") (1997). Düzeltilmiş çevrimiçi sürümü: (2006-) "Biocatalysis".
- ^ Faber, Kurt (2011). Biotransformations in organic chemistry a textbook (6th rev. and corr. ed.). Berlin: Springer-Verlag. ISBN 9783642173936.
- ^ Schmid, A.; Dordick, J. S.; Hauer, B.; Kiener, A.; Wubbolts, M.; Witholt, B. (2001). "Industrial biocatalysis today and tomorrow". Nature. 409 (6817): 258–268.. doi:10.1038/35051736 1 Eylül 2021 tarihinde Wayback Machine sitesinde arşivlendi. PMID 11196655
- ^ Müller, Michael (7 January 2005). "Chemoenzymatic Synthesis of Building Blocks for Statin Side Chains". Angewandte Chemie International Edition. 44 (3): 362–365. doi:10.1002/anie.200460852PMID 15593081
- ^ Berkessel, A.; Groeger, H. (2005). Asymmetric Organocatalysis. Weinheim: Wiley-VCH. ISBN 3-527-30517-3
- ^ Special Issue: List, Benjamin (2007). "Organocatalysis". Chemical Reviews 107 (12): 5413–5883. doi:10.1021/cr078412e
- ^ Gröger, Albrecht Berkessel; Harald (2005). Asymmetric organocatalysis – from biomimetic concepts to applications in asymmetric synthesis (1. ed., 2. reprint. ed.). Weinheim: Wiley-VCH. ISBN 3-527-30517-3.
- ^ Dalko, Peter I.; Moisan, Lionel (15 October 2001). "Enantioselective Organocatalysis". Angewandte Chemie International Edition. 40 (20): 3726–3748. doi:10.1002/1521-3773(20011015)40:20<3726::AID-ANIE3726>3.0.CO;2-D
- ^ Notz, Wolfgang; Tanaka, Fujie; Barbas, Carlos F. (1 August 2004). "Enamine-Based Organocatalysis with Proline and Diamines: The Development of Direct Catalytic Asymmetric Aldol, Mannich, Michael, and Diels−Alder Reactions". Accounts of Chemical Research. 37 (8): 580–591. doi:10.1021/ar0300468 26 Eylül 2018 tarihinde Wayback Machine sitesinde arşivlendi. PMID 15311957
- ^ Bertelsen, Søren; Jørgensen, Karl Anker (2009). "Organocatalysis—after the gold rush". Chemical Society Reviews. 38 (8): 2178–89. doi:10.1039/b903816g 25 Şubat 2019 tarihinde Wayback Machine sitesinde arşivlendi. PMID 19623342
- ^ Lakhtakia, A., ed. (1990). Selected Papers on Natural Optical Activity (SPIE Milestone Volume 15). SPIE.
- ^ Gal, Joseph (January 2011). "Louis Pasteur, language, and molecular chirality. I. Background and Dissymmetry". Chirality. 23(1): 1–16. doi:10.1002/chir.20866
- ^ Pasteur, L. (1848). "Researches on the molecular asymmetry of natural organic products, English translation of French original, published by Alembic Club Reprints (Vol. 14, pp. 1–46) in 1905, facsimile reproduction by SPIE in a 1990 book".
- ^ Pedro Cintas (2007). "Tracing the Origins and Evolution of Chirality and Handedness in Chemical Language". Angewandte Chemie International Edition. 46 (22): 4016–4024. doi:10.1002/anie.200603714 PMID 17328087
- ^ Le Bel, Joseph (1874). "Sur les relations qui existent entre les formules atomiques des corps organiques et le pouvoir rotatoire de leurs dissolutions" 19 Temmuz 2018 tarihinde Wayback Machine sitesinde arşivlendi. [On the relations which exist between the atomic formulas of organic compounds and the rotatory power of their solutions]. Bull. Soc. Chim. Fr. 22: 337–347.
- ^ van 't Hoff, JH (1874) "Sur les formülleri de yapı l'Espace dans" 10 Ocak 2020 tarihinde Wayback Machine sitesinde arşivlendi. , Archives Néerlandaises des Sciences Exactes ve Naturelles, 9 (yapısal alan formüller üzerinde) : 445-454.
- ^ a b c d e Koskinen, Ari M.P. (2013). Asymmetric synthesis of natural products (Second ed.). Hoboken, N.J.: Wiley. pp. 17, 28–29. ISBN 1118347331. Kaynak hatası: Geçersiz
<ref>etiketi: "Koskinen2012" adı farklı içerikte birden fazla tanımlanmış (Bkz: Kaynak gösterme) - ^ Fischer, Emil (1 October 1894). "Synthesen in der Zuckergruppe II". Berichte der deutschen chemischen Gesellschaft. 27 (3): 3189–3232. doi:10.1002/cber.189402703109
- ^ Fischer, Emil; Hirschberger, Josef (1 January 1889). "Ueber Mannose. II". Berichte der deutschen chemischen Gesellschaft. 22(1): 365–376. doi:10.1002/cber.18890220183
- ^ Marckwald, W. (1904). "Ueber asymmetrische Synthese". Berichte der deutschen chemischen Gesellschaft. 37: 349–354. doi:10.1002/cber.19040370165.
- ^ Campbell, Chantel D.; Vederas, John C. (23 June 2010). "Biosynthesis of lovastatin and related metabolites formed by fungal iterative PKS enzymes". Biopolymers. 93 (9): 755–763. doi:10.1002/bip.21428.
- ^ New Beer in an Old Bottle. Eduard Buchner and the Growth of Biochemical Knowledge, 1997
- ^ Bu erken dönem çalışmaların çoğu Almanca olarak yayınlandı, ancak çağdaş İngilizce hesapları Alexander McKenzie'nin makalelerinde bulunabilir, Koskinen (2012) gibi modern incelemelerde analizler ve yorumlar devam eder.
- ^ McKenzie, Alexander (1 January 1904). "CXXVII.Studies in asymmetric synthesis. I. Reduction of menthyl benzoylformate. II. Action of magnesium alkyl haloids on menthyl benzoylformate". J. Chem. Soc. Trans. 85: 1249. doi:10.1039/CT9048501249
- ^ Bijvoet, J. M.; Peerdeman, A. F.; van Bommel, A. J. (1951). "Determination of the Absolute Configuration of Optically Active Compounds by Means of X-Rays". Nature. 168 (4268): 271–272. Bibcode:1951Natur.168..271B. doi:10.1038/168271a0 6 Mayıs 2021 tarihinde Wayback Machine sitesinde arşivlendi.
- ^ Dalgliesh, C. E. (1952). "756. The optical resolution of aromatic amino-acids on paper chromatograms". Journal of the Chemical Society (Resumed): 3940. doi:10.1039/JR9520003940
- ^ Klemm, L.H.; Reed, David (1960). "Optical resolution by molecular complexation chromatography". Journal of Chromatography A. 3: 364–368. doi:10.1016/S0021-9673(01)97011-6 25 Şubat 2019 tarihinde Wayback Machine sitesinde arşivlendi.
- ^ Cushny, AR (2 November 1903)."Atropine and the hyoscyamines-a study of the action of optical isomers" The Journal of Physiology. 30 (2): 176–94. doi:10.1113/jphysiol.1903.sp000988. PMC 1540678. PMID 16992694 24 Şubat 2019 tarihinde Wayback Machine sitesinde arşivlendi..
- ^ Cushny, AR; Peebles, AR (13 July 1905). "The action of optical isomers: II. Hyoscines" 10 Ocak 2019 tarihinde Wayback Machine sitesinde arşivlendi. The Journal of Physiology. 32 (5–6): 501–10. doi:10.1113/jphysiol.1905.sp001097 30 Aralık 2021 tarihinde Wayback Machine sitesinde arşivlendi.. PMC 1465734 10 Ocak 2019 tarihinde Wayback Machine sitesinde arşivlendi.. PMID 16992790 24 Şubat 2019 tarihinde Wayback Machine sitesinde arşivlendi..
- ^ McBride, W. G. (1961). "Thalidomide and Congenital Abnormalities". The Lancet. 278 (7216): 1358. doi:10.1016/S0140-6736(61)90927-8. 25 Şubat 2019 tarihinde Wayback Machine sitesinde arşivlendi.
- ^ Robert Sidney Cahn; Christopher Kelk Ingold; Vladimir Prelog (1966). "Specification of Molecular Chirality". Angewandte Chemie International Edition. 5 (4): 385–415.
- ^ Vladimir Prelog; Günter Helmchen (1982). "Basic Principles of the CIP-System and Proposals for a Revision". Angewandte Chemie International Edition. 21 (8): 567–583. doi:10.1002/anie.198205671.
- ^ Gil-Av, Emanuel; Feibush, Binyamin; Charles-Sigler, Rosita (1966). "Separation of enantiomers by gas liquid chromatography with an optically active stationary phase". Tetrahedron Letters. 7(10): 1009–1015. doi:10.1016/S0040-4039(00)70231-0. 25 Şubat 2019 tarihinde Wayback Machine sitesinde arşivlendi.
- ^ Vineyard, B. D.; Knowles, W. S.; Sabacky, M. J.; Bachman, G. L.; Weinkauff, D. J. (1977). "Asymmetric hydrogenation. Rhodium chiral bisphosphine catalyst". Journal of the American Chemical Society. 99 (18): 5946–5952. doi:10.1021/ja00460a018.
- ^ Knowles, William S. (2002). "Asymmetric Hydrogenations (Nobel Lecture)". Angewandte Chemie International Edition. 41 (12): 1998. doi:10.1002/1521-3773(20020617)41:12<1998::AID-ANIE1998>3.0.CO;2-8.
- ^ Knowles, W. S. (March 1986). "Application of organometallic catalysis to the commercial production of L-DOPA". Journal of Chemical Education. 63 (3): 222. Bibcode:1986JChEd..63..222K. doi:10.1021/ed063p222. 20 Eylül 2018 tarihinde Wayback Machine sitesinde arşivlendi.
- ^ H. Nozaki; H. Takaya; S. Moriuti; R. Noyori (1968). "Homogeneous catalysis in the decomposition of diazo compounds by copper chelates: Asymmetric carbenoid reactions". Tetrahedron. 24 (9): 3655–3669. doi:10.1016/S0040-4020(01)91998-2. 25 Şubat 2019 tarihinde Wayback Machine sitesinde arşivlendi.
- ^ Katsuki, Tsutomu; Sharpless, K. Barry (1980). "The first practical method for asymmetric epoxidation". Journal of the American Chemical Society. 102 (18): 5974–5976. doi:10.1021/ja00538a077. 1 Ocak 2020 tarihinde Wayback Machine sitesinde arşivlendi.
- ^ Jacobsen, Eric N.; Marko, Istvan.; Mungall, William S.; Schroeder, Georg.; Sharpless, K. Barry. (1988). "Asymmetric dihydroxylation via ligand-accelerated catalysis". Journal of the American Chemical Society. 110 (6): 1968–1970. doi:10.1021/ja00214a053. 19 Eylül 2020 tarihinde Wayback Machine sitesinde arşivlendi.
- ^ Sharpless, K. Barry; Patrick, Donald W.; Truesdale, Larry K.; Biller, Scott A. (1975). "New reaction. Stereospecific vicinal oxyamination of olefins by alkyl imido osmium compounds". Journal of the American Chemical Society. 97 (8): 2305–2307. doi:10.1021/ja00841a071. 26 Haziran 2019 tarihinde Wayback Machine sitesinde arşivlendi.
- ^ J. A. Dale, D. L. Dull and H. S. Mosher (1969). "α-Methoxy-α-trifluoromethylphenylacetic acid, a versatile reagent for the determination of enantiomeric composition of alcohols and amines". J. Org. Chem. 34 (9): 2543–2549. doi:10.1021/jo01261a013 16 Ağustos 2021 tarihinde Wayback Machine sitesinde arşivlendi.
- ^ Hinckley, Conrad C. (1969). "Paramagnetic shifts in solutions of cholesterol and the dipyridine adduct of trisdipivalomethanatoeuropium(III). A shift reagent". Journal of the American Chemical Society. 91 (18): 5160–5162. doi:10.1021/ja01046a038. PMID 5798101
- ^ Ensley, Harry E.; Parnell, Carol A.; Corey, Elias J. (1978). "Convenient synthesis of a highly efficient and recyclable chiral director for asymmetric induction". The Journal of Organic Chemistry. 43 (8): 1610–1612. doi:10.1021/jo00402a037.
- ^ Sariaslani, F.Sima; Rosazza, John P.N. (1984). "Biocatalysis in natural products chemistry". Enzyme and Microbial Technology. 6(6): 242–253. doi:10.1016/0141-0229(84)90125-X. 25 Şubat 2019 tarihinde Wayback Machine sitesinde arşivlendi.
- ^ Wandrey, Christian; Liese, Andreas; Kihumbu, David (2000). "Industrial Biocatalysis: Past, Present, and Future". Organic Process Research & Development. 4 (4): 286–290. doi:10.1021/op990101l.